Comment le coronavirus tue-t-il?
Les cliniciens retracent un déchaînement féroce à travers le corps, du cerveau aux orteils
Par Meredith Wadman, Jennifer Couzin-Frankel, Jocelyn Kaiser, Catherine Matacic 17 avril 2020 à 18h45
Les rapports COVID-19 de Science sont pris en charge par le Pulitzer Center.
Lors de tournées dans une unité de soins intensifs de 20 lits un jour récent, le médecin Joshua Denson a évalué deux patients souffrant de convulsions, dont beaucoup souffraient d'insuffisance respiratoire et d'autres dont les reins étaient sur une dangereuse glissade en descente. Quelques jours plus tôt, ses tournées avaient été interrompues alors que son équipe tentait, sans succès, de réanimer une jeune femme dont le cœur s'était arrêté. Tous partageaient une chose, dit Denson, médecin pulmonaire et de soins intensifs à la faculté de médecine de l'Université de Tulane. «Ils sont tous positifs au COVID.»
Alors que le nombre de cas confirmés de COVID-19 dépasse 2,2 millions dans le monde et que les décès dépassent 150000, les cliniciens et les pathologistes ont du mal à comprendre les dommages causés par le coronavirus alors qu'il déchire le corps. Ils se rendent compte que bien que les poumons soient au point zéro, leur portée peut s'étendre à de nombreux organes, y compris le cœur et les vaisseaux sanguins, les reins, l'intestin et le cerveau.
«[La maladie] peut attaquer presque tout dans le corps avec des conséquences dévastatrices», déclare le cardiologue Harlan Krumholz de l'Université de Yale et de l'hôpital Yale-New Haven, qui mène de multiples efforts pour recueillir des données cliniques sur le COVID-19. «Sa férocité est époustouflante et humiliante.»
Comprendre le déchaînement pourrait aider les médecins en première ligne à traiter la fraction des personnes infectées qui deviennent désespérément et parfois mystérieusement malades. Une tendance dangereuse et nouvellement observée à la coagulation sanguine transforme-t-elle certains cas bénins en urgences potentiellement mortelles? Une réponse immunitaire trop zélée est-elle derrière les pires cas, suggérant qu'un traitement avec des médicaments immunosuppresseurs pourrait aider? Qu'est-ce qui explique le taux d'oxygène dans le sang étonnamment bas que certains médecins signalent chez des patients qui ne sont toujours pas à bout de souffle? «Adopter une approche systémique peut être bénéfique alors que nous commençons à penser aux thérapies», déclare Nilam Mangalmurti, intensiviste pulmonaire à l'hôpital de l'Université de Pennsylvanie (HUP).
Ce qui suit est un aperçu de la compréhension en évolution rapide de la façon dont le virus attaque les cellules autour du corps, en particulier chez environ 5% des patients qui deviennent gravement malades. Malgré les plus de 1000 articles qui se répandent maintenant dans les revues et sur les serveurs de pré-impression chaque semaine, une image claire est insaisissable, car le virus agit comme aucun pathogène que l'humanité n'a jamais vu. Sans études prospectives contrôlées plus vastes qui ne sont lancées que maintenant, les scientifiques doivent tirer des informations de petites études et de rapports de cas, souvent publiés à la vitesse de l'éclair et qui n'ont pas encore été examinés par des pairs. «Nous devons garder l'esprit très ouvert à mesure que ce phénomène progresse», déclare Nancy Reau, une transplantation hépatique qui a traité des patients atteints de COVID-19 au Rush University Medical Center. «Nous apprenons toujours.»
L'infection commence
Lorsqu'une personne infectée expulse des gouttelettes chargées de virus et que quelqu'un d'autre les inhale, le nouveau coronavirus, appelé SARS-CoV-2, pénètre dans le nez et la gorge. Il trouve une maison bienvenue dans la muqueuse du nez, selon une pré-impression de scientifiques de l'Institut Wellcome Sanger et d'ailleurs. Ils ont découvert que les cellules y sont riches en un récepteur de surface cellulaire appelé enzyme de conversion de l'angiotensine 2 (ACE2). Dans tout le corps, la présence d'ACE2, qui aide normalement à réguler la pression artérielle, marque les tissus vulnérables à l'infection, car le virus nécessite que ce récepteur pénètre dans une cellule. Une fois à l’intérieur, le virus détourne la machinerie de la cellule, faisant une myriade de copies de lui-même et envahissant de nouvelles cellules.
Au fur et à mesure que le virus se multiplie, une personne infectée peut en répandre de grandes quantités, en particulier au cours de la première semaine environ. Les symptômes peuvent être absents à ce stade. Ou la nouvelle victime du virus peut développer une fièvre, une toux sèche, un mal de gorge, une perte de l’odorat et du goût, ou des maux de tête et de corps.
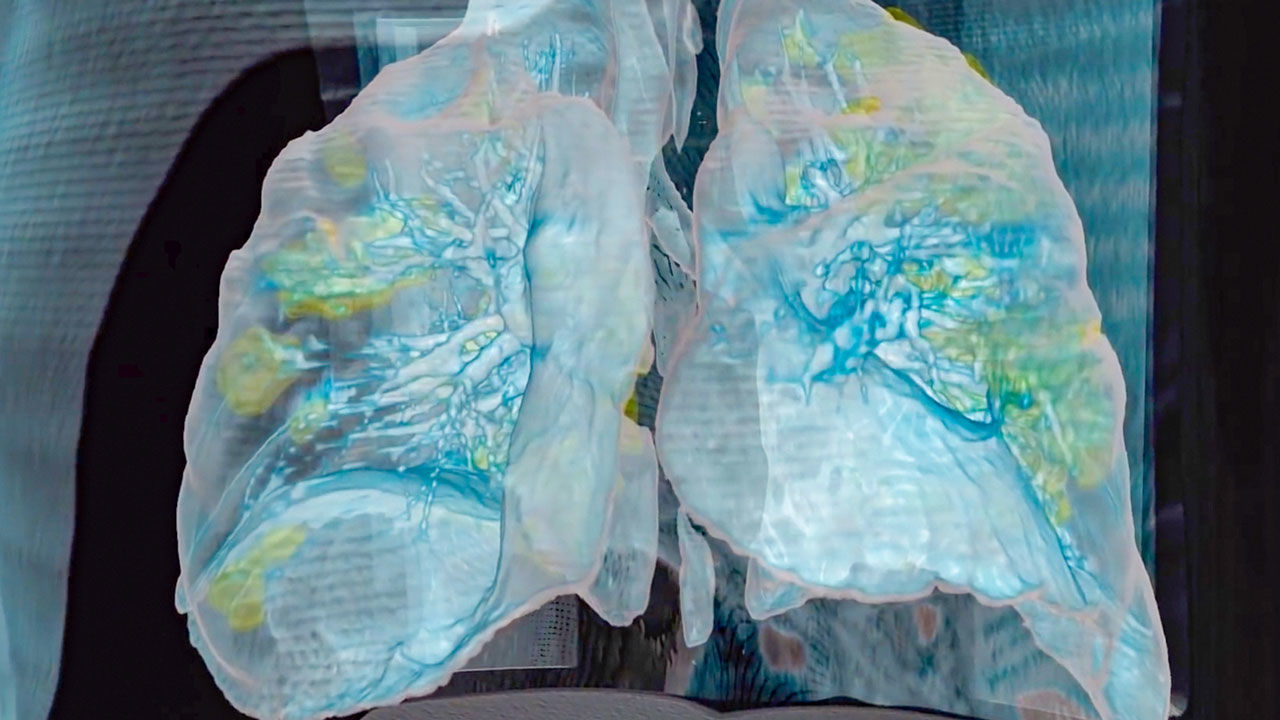
Si le système immunitaire ne repousse pas le SRAS-CoV-2 pendant cette phase initiale, le virus descend alors la trachée pour attaquer les poumons, où il peut devenir mortel. Les branches plus minces et éloignées de l’arbre respiratoire du poumon se terminent par de minuscules sacs aériens appelés alvéoles, chacun bordé d’une seule couche de cellules également riches en récepteurs ACE2.
Normalement, l'oxygène traverse les alvéoles dans les capillaires, de minuscules vaisseaux sanguins qui se trouvent à côté des sacs aériens; l'oxygène est ensuite transporté vers le reste du corps. Mais alors que le système immunitaire fait la guerre à l'envahisseur, la bataille elle-même perturbe ce transfert d'oxygène sain. Les globules blancs de première ligne libèrent des molécules inflammatoires appelées chimiokines, qui à leur tour invoquent davantage de cellules immunitaires qui ciblent et tuent les cellules infectées par le virus, laissant derrière elles un ragoût de liquide et de cellules mortes - du pus. C'est la pathologie sous-jacente de la pneumonie, avec ses symptômes correspondants: toux; fièvre; et respiration rapide et superficielle (voir graphique). Certains patients atteints de COVID-19 se rétablissent, parfois sans plus de soutien que l'oxygène respiré par les broches nasales.
Mais d'autres se détériorent, souvent assez soudainement, développant une condition appelée syndrome de détresse respiratoire aiguë (SDRA). Les niveaux d'oxygène dans leur sang chutent et ils ont de plus en plus de mal à respirer. Sur les radiographies et les tomodensitogrammes, leurs poumons sont criblés d'opacités blanches là où l'espace noir - l'air - devrait être. Généralement, ces patients se retrouvent sous ventilateurs. Beaucoup meurent. Les autopsies montrent que leurs alvéoles se sont remplies de liquide, de globules blancs, de mucus et de détritus de cellules pulmonaires détruites.
L'impact d'un envahisseur
Dans les cas graves, le SRAS-CoV-2 atterrit dans les poumons et peut y causer des dommages profonds. Mais le virus, ou la réponse du corps à celui-ci, peut endommager de nombreux autres organes. Les scientifiques commencent tout juste à sonder la portée et la nature de ce préjudice.
Cerveau : Certains patients atteints de COVID-19 ont des accidents vasculaires cérébraux, des convulsions, de la confusion et une inflammation du cerveau. Les médecins essaient de comprendre lesquels sont directement causés par le virus.
Yeux : La conjonctivite, inflammation de la membrane qui tapisse l'avant de l'œil et la paupière interne, est plus fréquente chez les patients les plus malades.
Nez : Certains patients perdent leur odorat. Les scientifiques pensent que le virus peut remonter les terminaisons nerveuses du nez et endommager les cellules.
Poumons : Une coupe transversale montre des cellules immunitaires encombrant une alvéole enflammée, ou un sac d'air, dont les parois se décomposent lors de l'attaque du virus, diminuant la consommation d'oxygène. Les patients toussent, la fièvre augmente et la respiration devient difficile.
Coeur et vaisseaux sanguins : Le virus pénètre dans les cellules, y compris probablement celles qui tapissent les vaisseaux sanguins, en se liant aux récepteurs de l'enzyme de conversion 2 (ACE2) de l'angiotensine à la surface cellulaire. L'infection peut également favoriser les caillots sanguins, les crises cardiaques et l'inflammation cardiaque.
Foie: jusqu'à la moitié des patients hospitalisés ont des taux d'enzymes qui signalent un foie en difficulté. Un système immunitaire en surmultiplication et des médicaments administrés pour combattre le virus peuvent être à l'origine des dommages.
Rein : Les lésions rénales sont fréquentes dans les cas graves et rendent la mort plus probable. Le virus peut attaquer directement les reins, ou une insuffisance rénale peut faire partie d'événements du corps entier comme la chute de la pression artérielle.
Intestins: Les rapports des patients et les données de biopsie suggèrent que le virus peut infecter le tractus gastro-intestinal inférieur, qui est riche en récepteurs ACE2. Environ 20% ou plus des patients souffrent de diarrhée.
Certaines études ont montré des taux élevés de ces cytokines induisant une inflammation dans le sang des patients hospitalisés COVID-19. «La morbidité et la mortalité réelles de cette maladie sont probablement dues à cette réponse inflammatoire disproportionnée au virus», déclare Jamie Garfield, un pneumologue qui s'occupe des patients COVID-19 au Temple University Hospital.
Mais d’autres ne sont pas convaincus. «Il semble y avoir eu un mouvement rapide pour associer le COVID-19 à ces états hyperinflammatoires. Je n’ai pas vraiment vu de données convaincantes indiquant que tel est le cas », déclare Joseph Levitt, médecin de soins intensifs en pneumologie à la Stanford University School of Medicine.
Il craint également que les efforts visant à atténuer une réponse cytokine ne se retournent contre eux. Plusieurs médicaments ciblant des cytokines spécifiques sont en cours d'essais cliniques chez des patients atteints de COVID-19. Mais Levitt craint que ces médicaments ne suppriment la réponse immunitaire dont le corps a besoin pour combattre le virus. "Il y a un risque réel que nous autorisions une réplication virale plus importante", dit Levitt.
Pendant ce temps, d'autres scientifiques se concentrent sur un système organique totalement différent qui, selon eux, est à l'origine de la détérioration rapide de certains patients: le cœur et les vaisseaux sanguins.
Les craintes mondiales de pénurie de ventilateurs pour les poumons défaillants ont reçu beaucoup d'attention. Pas si un brouillage pour un autre type d'équipement: les machines de dialyse. «Si ces personnes ne meurent pas d’une insuffisance pulmonaire, elles meurent d’une insuffisance rénale», déclare la neurologue Jennifer Frontera du Langone Medical Center de l’Université de New York, qui a traité des milliers de patients atteints de COVID-19. Son hôpital développe un protocole de dialyse avec différentes machines pour prendre en charge des patients supplémentaires. La nécessité d'une dialyse peut être due au fait que les reins, abondamment dotés de récepteurs ACE2, présentent une autre cible virale.
Selon une prépublication, 27% des 85 patients hospitalisés à Wuhan avaient une insuffisance rénale. Un autre a rapporté que 59% des près de 200 patients hospitalisés sous COVID-19 dans les provinces chinoises du Hubei et du Sichuan avaient des protéines dans leurs urines et 44% avaient du sang; les deux suggèrent des lésions rénales. Ceux qui souffraient d'une lésion rénale aiguë (AKI) étaient plus de cinq fois plus susceptibles de mourir que les patients atteints de COVID-19 sans elle, selon la même pré-impression chinoise.

Une femme de 58 ans atteinte du COVID-19 a développé une encéphalite, entraînant des lésions tissulaires dans le cerveau (flèches).
N. Poyiadji et al., Radiologie, (2020) doi.org/10.1148/radiol.2020201187
Mais d'autres facteurs pourraient endommager le cerveau. Par exemple, une tempête de cytokines pourrait provoquer un gonflement du cerveau, et la tendance exagérée du sang à coaguler pourrait déclencher des accidents vasculaires cérébraux. Le défi est maintenant de passer de la conjecture à la confiance, à un moment où le personnel se concentre sur le sauvetage de vies, et même les évaluations neurologiques comme l'induction du réflexe nauséeux ou le transport de patients pour des scintigraphies cérébrales risquent de propager le virus.
Le mois dernier, Sherry Chou, neurologue au centre médical de l'Université de Pittsburgh, a commencé à organiser un consortium mondial qui comprend désormais 50 centres pour extraire des données neurologiques des soins que les patients reçoivent déjà. Les premiers objectifs sont simples: identifier la prévalence des complications neurologiques chez les patients hospitalisés et documenter leur état de santé. À plus long terme, Chou et ses collègues espèrent recueillir des scans, des tests de laboratoire et d’autres données pour mieux comprendre l’impact du virus sur le système nerveux, y compris le cerveau.
Chou spécule sur une possible voie d'invasion: par le nez, puis vers le haut et à travers le bulbe olfactif - expliquant les rapports d'une perte d'odeur - qui se connecte au cerveau. «C’est une belle théorie», dit-elle. «Nous devons vraiment aller le prouver.»
La plupart des symptômes neurologiques «sont signalés d'un collègue à l'autre par le bouche à oreille», ajoute Chou. «Je ne pense pas que quiconque, et certainement pas moi, puisse dire que nous sommes des experts.»
Atteindre l'intestin
Début mars, une femme du Michigan de 71 ans est revenue d'une croisière sur le Nil avec une diarrhée sanglante, des vomissements et des douleurs abdominales. Au départ, les médecins soupçonnaient qu'elle avait une punaise abdominale commune, telle que Salmonella. Mais après avoir développé une toux, les médecins ont prélevé un prélèvement nasal et l'ont trouvée positive pour le nouveau coronavirus. Un échantillon de selles positif pour l'ARN viral, ainsi que des signes de lésion du côlon observés lors d'une endoscopie, ont indiqué une infection gastro-intestinale (GI) par le coronavirus, selon un article publié en ligne dans The American Journal of Gastroenterology (AJG).
Son cas s'ajoute à un nombre croissant de preuves suggérant que le nouveau coronavirus, comme son cousin le SRAS, peut infecter la muqueuse du tube digestif inférieur, où les récepteurs ACE2 cruciaux sont abondants. L'ARN viral a été trouvé dans pas moins de 53% des échantillons de selles des patients prélevés. Et dans un article sous presse à Gastroenterology, une équipe chinoise a rapporté avoir trouvé la coque protéique du virus dans des cellules gastriques, duodénales et rectales dans des biopsies d'un patient COVID-19. «Je pense qu'il se reproduit probablement dans le tractus gastro-intestinal», explique Mary Estes, virologue au Baylor College of Medicine.
Source : https://www.sciencemag.org/news/2020/04/how-does-coronavirus-kill-clinicians-trace-ferocious-rampage-through-body-brain-toes#




Comments est propulsé par CComment